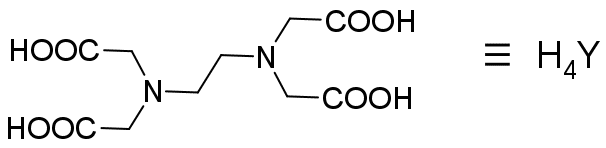
エチレンジアミン四酢酸
EDTA(エチレンジアミン四酢酸)は、 キレート剤(コンプレクサン complexane (Komplexon®)とも。 工業的には金属封鎖剤などとも呼ばれます)の代表格で、キレート滴定で多用されます。 しばしば中性の分子種を H4Y と略記します。 塩基として考えると H5Y+ などという分子種もあり得ますが、 これは強酸で、通常は H4Y の解離平衡(H4Y ⇌ H+ + H3Y-)を 第 1 解離 pK1 として表します。 pK1 = 2.0 で以下 pK2 = 2.67、 pK3 = 6.16、 pK4 = 10.26 とされています。 後のキレート錯体の生成定数とも関わりますが pH 10 程度以上で Y4- が主要なイオン種になることは記憶しておいてよいことです。 ここでは種々の金属イオンとの EDTA のキレート錯体生成定数と、 キレート滴定の際に使用される指示薬(金属指示薬)についてまとめておきます (このページのデータは上野景平「キレート滴定法」、南江堂、改訂版 1972 によります)。
なお遊離酸 EDTA H4Y の固体は、常温で難溶性で(溶解度 0.3 mass% 程度)、 通常は二ナトリウム塩の二水塩 Na2H2Y·2H2O (Na2C10H14N2O8·2H2O) の形で使用されます。 二ナトリウム塩二水塩の結晶は常温で安定で、 純度の高い試薬が容易に入手できます。
EDTA は種々の金属イオンと 1:1 のキレートを生成します。 表 1 に EDTA のキレート生成反応
Mn+ + Y4- ⇌ MY(n-4)+
の平衡定数(安定度定数)の対数 log K をまとめました(20 °C、イオン強度 0.1 mol/L が中心)。
| 金属イオン | log K | 金属イオン | log K | 金属イオン | log K | 金属イオン | log K | |||
|---|---|---|---|---|---|---|---|---|---|---|
| Li+ | 2.8 | Ca2+ | 10.70 | Co2+ | 16.31 | Cu2+ | 18.80 | |||
| Ag+ | 7.32 | Mn2+ | 13.79 | Zn2+ | 16.50 | Hg2+ | 21.80 | |||
| Ba2+ | 7.76 | Fe2+ | 14.33 | Pb2+ | 18.04 | Fe3+ | 25.1 | |||
| Mg2+ | 8.69 | Al3+ | 16.13 | Ni2+ | 18.62 | Co3+ | 36 |
EDTA によるキレート滴定で、当量点を判別するのに金属指示薬と呼びれる指示薬を使用します。 金属指示薬 X は、金属イオン M と錯体 MX を作って変色します。
M + X ⇌ MX KMX = [MX]/([M][X])
たいていの場合、金属イオンの種類によらず、MX は同じ色調を示します。 EDTA 濃度の変化に応じて遊離の金属イオン M が変化し、X と MX の濃度比が変化、 その色の変化を捉えて当量点を判別するわけです。 目視で判断することを考えると、典型的には [X] + [MX] は 10-6 mol/L のオーダーになります。 またそれが滴定で検知できる限界濃度です。
キレート滴定で金属イオン N を EDTA(Y と略記)で滴定することを考えます(N は必ずしも M と同じではない)。
N + Y ⇌ NY KNY = [NY]/([N][Y])
M + Y ⇌ MY KMY = [MY]/([M][Y]) (≫ KMX)
金属指示薬 X が有効に機能するには、まず滴定初期に MX の形で存在している必要があります ([MX]/[X] = KMX[M]0 ≫ 1)。 そして EDTA を滴下していったとき、当量点近傍では N(や M)とキレートを作っていない EDTA の濃度 [Y] が増加し MX が減少する。 つまり MX + Y → X + MY の反応が進行し MX の色が消失します。 [MX]/[MY] = (KMX/KMY) ([X]/[Y]) ですから、 KMX ≪ KMY である必要があります。
こうした要件と同時に、pH によっても金属指示薬は変色します(X が M の代わりに H+ と結合する)。 また生成した MX の解離速度が遅いなどといった事態もあったりします。 金属指示藥の選定は、pH や滴定手法(逆滴定や置換滴定など)も含め、慎重に行う必要があり、 すでに膨大な研究が積み上げられています。 ここには学生実験と関わる金属指示薬について紹介します。
| 指示薬 | 変色 | 使用可能 pH* | 被滴定金属例** |
|---|---|---|---|
| EBT | 赤 → 青 | 7 ~ 10 | Mg, Ca, Mn, Zn, [Co, Ni, Cu] |
| NN | 赤 → 青 | 12 ~ | Ca |
| XO | 赤 → 黄 | ~ 6 | Zn, Pb, [Al] |
| Cu-PAN | 赤紫 → 黄 | 2 ~ 11 | Al, Zn, Ni, Co, |