|
化学反応には、色の変化、固体の析出といった目に見える変化のないものも多く、 反応容器の中で何が起こっているか、見た目だけでは判別が容易でありません。 このため有機合成では、安価で簡便な上、短時間で反応容器内の多くの情報が得られる優れた分析方法として、 薄層クロマトグラフィー(TLC。Thin Layer Chromatography)が汎用されています。 TLC は、プラスチック等の板に塗布されたシリカゲルやアルミナの細粉中に溶媒が浸透していく過程で、 溶質が分離されていくことを利用します。 分取を目的とするカラムクロマトグラフィーより細かいシリカゲルやアルミナ粉末を用いるので、 分離能はより高くなります。
まずは TLC の手順を簡単にまとめておきましょう。
最近はスマホで写真を撮って、スポットの位置の解析までやってくれるアプリもあります。 大いに利用してもらえばいいでしょう。
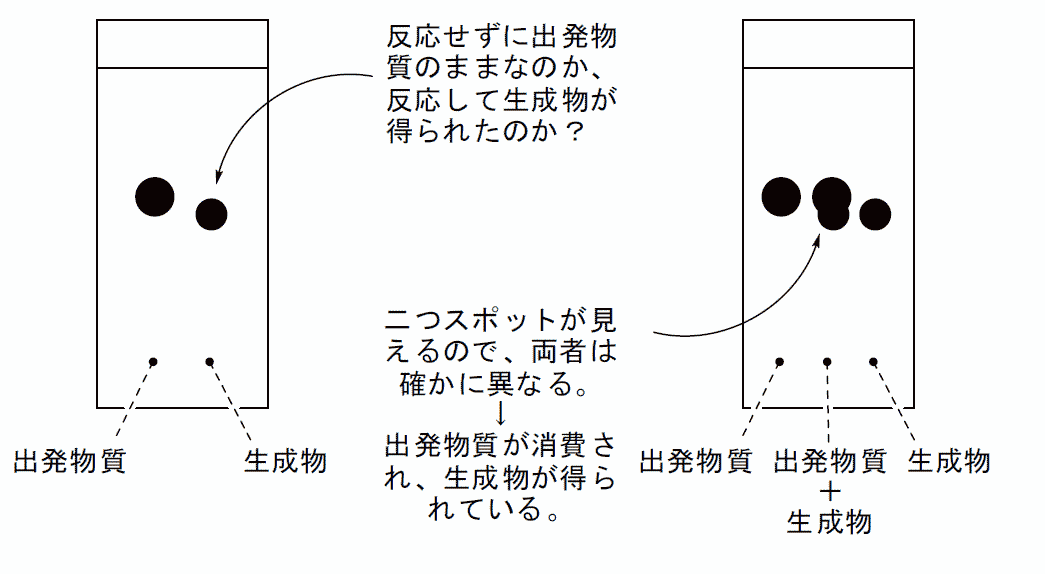
溶離液が上昇してきた距離 LS とその時試料が到達した距離 LX の比 LX/LS を Rf 値(retardation factorあるいはrate of flow)と呼びます。 Rf 値はその時々の実験条件によってかなり変化します。 有機合成実験で TLC を用いるときは、Rf 値自身ではなく、 反応や精製操作等による各スポットの消長が重要であり、TLC を行う際には、 比較対象となるものを同時に展開することが一般に行われます。 反応を追跡する場合には、反応物と生成物の重ね打ちが有効です。
もともと出発物質と生成物の Rf 値の差が小さかったり、 展開溶媒が水平に上がらなかったりすると、全く異なる物質であっても似た Rf 値を示したり、 同一の物質であっても若干異なる Rf 値を示したりすることがあります。 そこで、下のように出発物質と生成物を重ね打ちすることで、 両者が異なるものであるかが、判然と確認できるわけです。
| 溶離能 | 溶媒 |
|---|---|
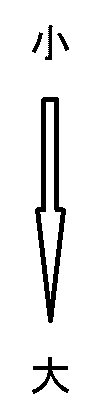 | ヘキサン |
| トルエン | |
| エチルエーテル | |
| クロロホルム | |
| アセトン | |
| 酢酸エチル | |
| アセトニトリル | |
| エタノール | |
| メタノール | |
| 水 |
学生実験で使用する TLC は、シリカゲルを担体に用いているので、 極性の高い溶剤ほど大きな Rf 値を与える傾向があります(いわゆる順相のクロマトグラフィー)。 溶離能の順に溶媒を並べた溶離列 elutropic series と呼ばれるものが知られています。 展開にともなう組成変化がないので純溶媒の方が分離能は高いのですが、 実用的には、溶媒の種類が少なくて済むヘキサン-酢酸エチル(極性の高い物質についてはクロロホルム-メタノール)などの混合溶媒が、 混合比をさまざまに変えて、よく使われています。
なお溶離能だけではなく、(金額は当然のことながら)、 溶媒の粘度や表面張力も TLC の展開に要する時間を節約する上では重要で(時間がかかり過ぎると反応が終わってしまう)、 溶媒の選択には、分野により人により、いろいろ流儀があるようです。 困ったときは実験書や経験豊かな先輩に聞くのがよいでしょう。
TLCのスポットの検出にはさまざまな手法が用いられますが、 学生実験では蛍光の消光を利用します。 学生実験で用いる TLC プレートのシリカゲルにはあらかじめ蛍光物質が入っていて、 紫外線を照射すると緑色に光ります。 多くの有機物はその発光を妨げるので、ブラックライトで紫外線を照射すると、有機物の存在する場所は黒く浮いて見えます。
使用するブラックライトから出る紫外線のスペクトルは右図のようなもので、 可視光領域(400 nm以上)にはほとんど強度がありません。 目で見て弱い光と感じても、有害な 315 nm以下の紫外線(UV-B、UV-Cと呼ばれるもの)が出ています。 無用に紫外線を浴びないように注意してください。
なお紫外部に光吸収を示さず、消光を示さないものもあります。 そうした場合には、ヨウ素による呈色を利用する方法、 硫酸やモリブドリン酸を噴霧して加熱呈色させる方法、 アミノ酸であればニンヒドリン反応を利用するなど、 さまざまな手法が用いられます。