|
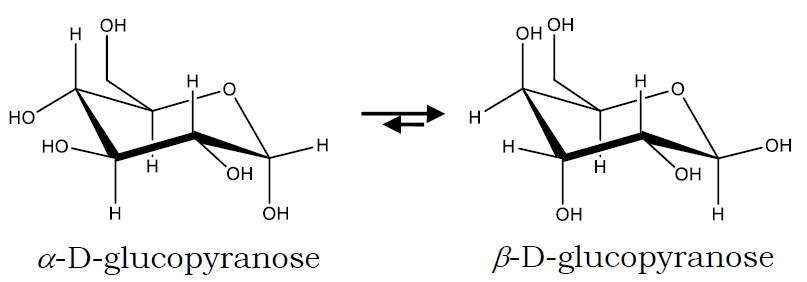
| 図4A. グルコースの互変異性平衡 |
ショ糖を加水分解し旋光度や反応性の変化を調べる。
ショ糖1分子を加水分解するとグルコースとフルクトースそれぞれ1分子が生成する。 ショ糖、グルコースは右旋性を示す([α]D は ショ糖が+66°、グルコースが+53°)のに対し、 フルクトースは大きな左旋性を示す(-92°)ため、 加水分解することで旋光能が + から - に変化する。 このためショ糖を加水分解して生成するグルコースとフルクトースの混合糖を転化糖と呼ぶ。 転化糖は清涼飲料水等に広く用いられ、料理に用いられる上白糖にも含まれている。
旋光能(比旋光度) [α]D は通常 1 g/mL 濃度の溶液で 10 cm 通過する間に何度偏光面が回転するかで表される(D はナトリウムの D線(590 nm)を意味する)。 したがって10 %のショ糖溶液を長さ10 cm程度の試験管に入れた場合の旋光度は7° 程度である。

|
| 図4A. グルコースの互変異性平衡 |
なおグルコースやフルクトースは溶液中で α型と β型の間の互変異性平衡が生じており、 結晶を溶解すると時間とともに旋光能が変化する(変旋光 mutarotation)。 興味のあるものはフルクトースの結晶を溶かした溶液の旋光度の変化を調べてみよ。
糖類一般の検出法として、ここに取り上げるアントロン反応とモーリッシュ反応は代表的なものである。 発色の原理は必ずしも明確ではないが、濃硫酸によって糖が分解されフルフラール類縁化合物ができ、 それがアントロンやナフトールと反応して発色しているものと推測される。 なおケトースの呈色反応であるセリワノフ反応はケトースが塩酸と反応してヒドロキシメチルフルフラール類縁化合物となることを利用している。 ただしアルドースも長時間反応させると呈色し、ショ糖は加水分解してフルクトースを生成して呈色する。
還元糖の検出法としては、ここでも取り上げるフェーリング反応と銀鏡反応が代表的である。 他にもベネディクト反応(フェーリング反応より温和な条件で銅(II)の還元を見る)や バーフォード Barfoed反応(さらに温和な二糖類が反応しないような条件)が知られている。
なお糖の検出対象には通常0.1 %以下の濃度を問題にすることが多い(血糖値はおよそ100 mg/dL ~ 0.1 %程度)。 ここでは明瞭な反応が出るように高めの濃度の設定になっている。
ここではショ糖の塩酸による加水分解を行うが、デンプンは今回のような条件では容易に加水分解されない。 しかし酵素を用いれば容易に加水分解が可能である。
興味のあるものは「新タカヂア錠」を擂り潰したもの(あるいはジャスターゼ)を4 %デンプン溶液(糊)に加えて混合して変化を観察してみよ。 また酵素で処理した溶液についてフェーリング反応を試してみよ。
糖に関する実験は、 生体関連物質に関わる課題として、 入門化学実験のスタート時点から組み込んでいました。 アミノ酸や脂肪なども取り上げようという欲張った構成も考えたりしたのですが、 生体関連物質の特徴でもある光学活性に関わるものとして、転化糖の問題を取り上げることにしました。 また最初の内は糖の定性試験を、転化糖になって還元性を示すようになるのをチェックする(フェーリング反応や銀鏡反応が陽性)という形で入れていました。 けれども高校レベルで足踏みしているのは残念で、2012 年度から少し進んだ定性試験も取り入れ、 課題名も「ショ糖の転化」から現在の「ショ糖の転化・糖の定性反応」に変更しました。
話が長くなるので、この課題の詳細については、 下記サイトを参照ください。