last revised 2023.7 / 2020.3
吉村洋介
入門化学実験
4B. 化学振動反応
予習チェックのページへ
種々の化学反応が組み合わさることによって、振動的な挙動を示す化学反応系が存在する。
4B-1. 時計反応
<試薬・材料>
- 0.10 mol/L ヨウ素酸カリウム(KIO3)溶液
- 0.10 mol/L 亜硫酸水素ナトリウム(NaHSO3)溶液
- AC-AC アダプター(15 V/100 V)
- マルチメータ(Agilent U1251A)
<操作>
- 用意してある 0.10 mol/Lヨウ素酸カリウム溶液、0.10 mol/L 亜硫酸水素ナトリウム溶液を、
それぞれ 3 mL 程度試験管に取り、水を加えて5倍に希釈する。
以下この 0.02 mol/L程度に希釈した溶液をそれぞれ KIO3液、NaHSO3液と呼ぶ。
- 調製した溶液と水を、次のような容量比で混合した時、
ヨウ素の褐色が出現するまでの時間(誘導時間)を調べよ。デンプン溶液を加えて呈色を明瞭にしてもよい。
| KIO3液 | NaHSO3液 | 水 |
| ア | 2 | 2 | 1 |
| イ | 2 | 1 | 2 |
| ウ | 1 | 1 | 3 |
- KIO3液:NaHSO3液:水 = 1:1:5の時、呈色するのにかかる時間を予想し実際に試してみよ。
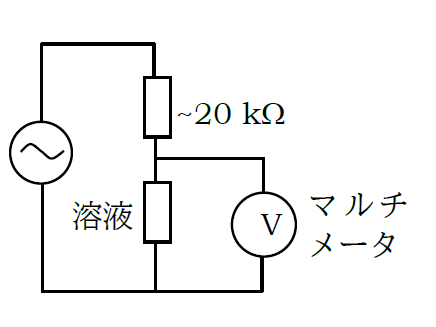
- 50 mL程度のビーカーに水 20 mL、NaHSO3液 4 mL を取り電極を浸し、図のような回路を組む。
- KIO3液 4 mL を加えて混合し、溶液にかかる電圧の変化をデータロガーを用いて記録し(参考4-5参照)、
電気伝導度の変化をモニターする。
4B-2. ベロウソフ-ザボチンスキー Belousov-Zhabotinsky 反応
<試薬・材料>
- 0.30 mol/L 臭素酸カリウム(KBrO3)溶液
- 0.35 mol/L マロン酸(CH2(COOH)2)溶液
- 0.010 mol/L 硫酸セリウム(IV)アンモニウム(Ce(NH4)4(SO4)4·2H2O)溶液
以上いずれも2 N 硫酸溶液。
- フェロイン([Fe(Phen)3]SO4)溶液(0.5 %)
- ルテニウム錯体( [Ru(bpy)3]Cl3)溶液(0.5 %)
<操作>
- 臭素酸カリウム、マロン酸溶液を、それぞれ 1 mL ずつサンプル管に取って混ぜ、回転子を入れてマグネチックスターラーで撹拌する。
ここに硫酸セリウム(IV)アンモニウム溶液を 1 mL 加える。
- しばらくすると色の変動が始まるので、変動の周期を記録する。
- 振動を見やすくするため、フェロイン溶液あるいはルテニウム錯体溶液を数滴加え、同様に変化を観察する。
4Be. 「化学振動反応」の背景
4Be-1. 時計反応
さまざまな時計反応が知られているが、ここでは古典的なヨウ素酸カリウムと亜硫酸水素ナトリウムの時計反応を取り上げる:
2IO3- + 5 HSO3- + 2H+ → I2 + 5 HSO4- + H2O
この反応は大きく次の3つの過程からなっていると考えられている:
- IO3- + 3 HSO3- → I- + 3 HSO4- (1)
- IO3- + 6 H+ + 5 I- → 3I2 + 3 H2O (2)
- 3I2 + 3 HSO3- + 3 H2O → 6I- + 6 H+ + 3 HSO4- (3)
|
|
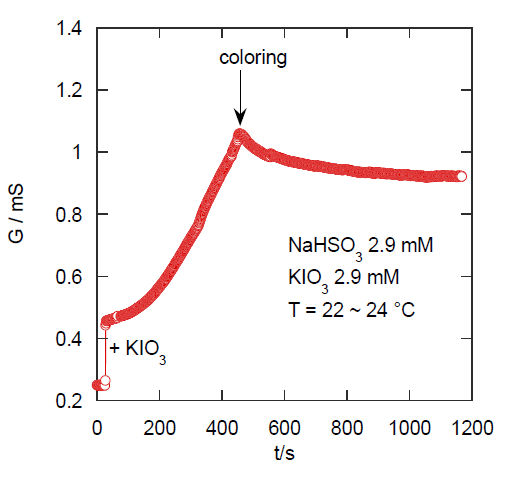
図4B. 典型的な時計反応の電気伝導度変化
|
この中の(3)の反応は比較的速やかに起きる。(2)で生じたヨウ素が(3)で消費され、反応初期ではヨウ化物イオンが蓄積されていくが、
反応進行とともに亜硫酸が失われ(3)の反応が終息するとともに、
ヨウ素の出現が観察されることになる((2)+(3)で(1)の反応になることに注意)。
時計反応における電気伝導度の時間変化の典型的な測定結果を図4Bに示す。
水溶液中の水素イオンの電気伝導度は大きく、他のイオンの電気伝導度の5倍程度ある。
このため反応初期の亜硫酸を消費しヨウ化物イオンが蓄積されていく過程では、水素イオン濃度の増加にともなって電気伝導度は増加し、
亜硫酸が消費されてしまうと(2)の反応による水素イオン濃度の減少のために電気伝導度は減少する。
4Be-2. 化学振動反応
化学振動反応として有名なベロウソフ-ザボチンスキー(BZ)反応を取り上げる。
化学振動反応の一つのポイントは、電気回路で言えば発振回路に組み込まれている「増幅回路」がどうなっているかにある。通常、化学反応が起きると、反応物の濃度が減少するが、それではたとえ振動しても急速に減衰して、振動としてはほとんど観測できない。したがって
X + Y → 2X + Z
のような増幅反応(通常、自己触媒反応と呼ぶ)が組み込まれていることが、化学振動を起こす上で必須と言ってよい。
BZ反応では、最終的には臭素酸イオン BrO3- がマロン酸等で還元され臭化物イオンBr-になるが、
中間に生成する亜臭素酸 HBrO2 に関する自己触媒反応が起きるというシナリオが流布されている:
HBrO2 + BrO3- + 2Ce3+ + 3H+ → 2HBrO2 +2Ce4+ + H2O
この自己触媒反応が、さらにさまざまなプロセスと関わって、最終的に化学振動を演出することになる。
「化学振動反応」のこと
当初から、反応速度の課題を入れることにしていたのですが、
どのような反応系を選ぶのかは問題です。
エステルの加水分解などの、お行儀のいい(「教育的」な)反応もあるでしょうが、
入門化学実験としては、もっと化学反応の広がり・可能性を感じさせるものがよいだろうと考えています。
そこで高校の科学クラブなどでもよく取り上げられている(と思われる)
化学振動反応に取材しています。
けれども化学振動はそのメカニズムの取り扱いが厄介なので(ぼくには理解できていないので)、
もう少し内実に迫ることのできる複合反応として、その代表格とも言える古典的な時計反応(ランドルト反応)を組み合わせて、
一つの課題にしています。
こうした単調でない挙動を示す複合反応については、
以前、学生実験の担当になる前から、3回生の反応速度の課題に関わって、
いくつかの反応系の課題を構成したことがありました。
時計反応もその一つで、2016 年度まで3回生の実験でも「任意課題」の形で行っていました
(現在はアセトンとヨウ素の反応に変更)。
入門化学実験ではその設定を、スケールなど変更して引き継いでいます。
実は当初の入門化学実験では、BZ 反応の構成要素でもあるハロゲンとカルボニル化合物の反応という流れで、
時計反応ではなく、アセトンとヨウ素の反応を取り上げていました。
けれどもちょっと理屈っぽい課題のせいか、学生さんの受けがあまり良くなくて、2012 年度の後期から時計反応に変更しました。
化学振動の課題の設定については「振動反応と時計反応(教師のための化学実験 ケミカルデモンストレーション6)」
(B. Z. Shakhashiri 著、池本 勲訳 丸善 1998。
ISBN 978-4621045176)を参考にしました。
このシリーズはよくできた本ですが、なぜか絶版なのは残念
(原著は今も刊行されています。振動反応は原著シリーズの第 2 巻、
時計反応は第 4 巻)。
|
|
|
図5. アセチルアセトンを用いた BZ 反応
(臭素酸酸化、マンガン触媒。フェロイン添加)の実験の様子。
|
化学振動反応としては、
ベロウソフ-ザボチンスキー(BZ)反応が古くから知られ、
振動するパラメータ領域が広く、振動挙動が安定していて、
学生実験で取り上げるには適切だと思います。
さまざまな変形版がありますが、
当初は手持ちの試薬で間に合わせ、
硫酸マンガンを触媒にアセチルアセトンを臭素酸カリで酸化するというものでした。
実際に実施してみると、
これまでやったことがないという学生が大半で、
当方が思っていた以上に学生さんの反応はよかったです(図 5 )。
けれども少しの混合比の変動で化学振動が不鮮明になったり、また反応が進むにつれ不溶性の物質ができて溶液が濁るので、
2012 年度からはマロン酸を使用するようにしました。
またマンガン触媒だと化学振動が起きる濃度領域が狭いようで、振動が容易に起きないケースもあり、
2015 年度から元祖セリウム触媒の BZ 反応にしています。
また無論、要望があれば、(できる範囲で)ブリッグズ-ラウシャー反応など、さまざまな振動反応に挑戦するようにしています。
最近はそういう要望を受けることもなくなりましたが・・・
例によって話が長くなるので、この課題の詳細については、
下記サイトを参照ください。
目次のページへ